Le système Edison d’histotripsie d’HistoSonics obtient un accès anticipé au marché britannique dans le cadre d’une autorisation pour besoins cliniques non satisfaits
Traitement non invasif des tumeurs du foie reconnu par l'Innovative Devices Access Pathway (IDAP) du Royaume-Uni
MINNEAPOLIS--(BUSINESS WIRE)--HistoSonics a annoncé aujourd’hui que son système Edison d'histotripsie, conçu pour la destruction non invasive des tumeurs hépatiques, a obtenu un accès anticipé limité et contrôlé au marché en Grande-Bretagne dans le cadre d’une autorisation pour besoins cliniques non satisfaits (Unmet Clinical Need Authorisation – UCNA). Cette désignation, rendue possible par le programme britannique Innovative Devices Access Pathway (IDAP), garantit un accès précoce et contrôlé à la technologie de l’histotripsie pour certains patients atteints de tumeurs hépatiques, marquant une étape importante dans l’élargissement des options de traitement pour l’un des besoins médicaux non satisfaits les plus urgents en oncologie au Royaume-Uni.



Le programme IDAP, lancé par le gouvernement britannique pour stimuler l’intégration des technologies médicales innovantes dans le système de santé, a sélectionné le système Edison comme l’un des huit seuls dispositifs retenus en 2024, en raison du potentiel de l’histotripsie à répondre de manière substantielle aux besoins de santé actuels et futurs les plus importants du Royaume-Uni. À l’issue d’un processus d’évaluation rigoureux, l’organisme britannique de réglementation des dispositifs médicaux (la Medicines and Healthcare products Regulatory Agency – MHRA) a déterminé que nos dispositifs d’histotripsie pouvaient être mis à disposition dans le cadre d’une UCNA, soulignant ainsi l’importance que pourrait avoir cette technologie pour la santé publique, notamment pour les patients atteints de tumeurs hépatiques primaires ou métastatiques.
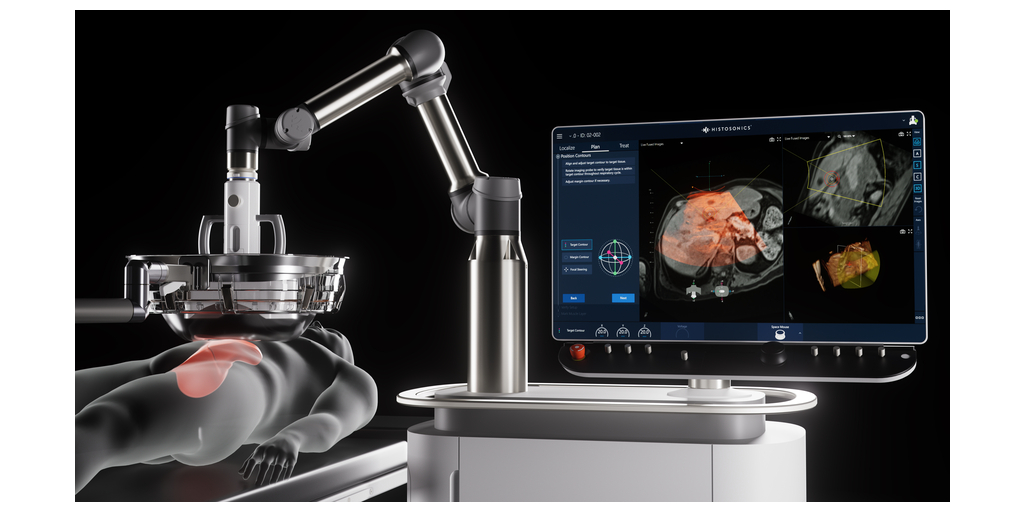
Le système Edison est la première et la seule plateforme à utiliser l’histotripsie – une technologie non thermique et non invasive basée sur les ultrasons focalisés – pour liquéfier mécaniquement les tumeurs, sans chirurgie, sans radiothérapie ni traitements systémiques. L’appareil a obtenu une autorisation De Novo de la Food and Drug Administration (FDA) des États-Unis en octobre 2023. La plateforme d’HistoSonics permet aux médecins de planifier, cibler, traiter et surveiller la destruction des tumeurs avec une visualisation permanente en temps réel et un contrôle constant, offrant un niveau de précision et de maîtrise inégalé par toute autre modalité existante.
« L’obtention d’un accès contrôlé en Grande-Bretagne dans le cadre du programme pilote IDAP représente une étape majeure pour HistoSonics et témoigne d’une reconnaissance claire du potentiel de notre technologie à impacter les soins médicaux », a déclaré Mike Blue, président et PDG d’HistoSonics. « Nous sommes honorés de collaborer avec le NHS ainsi qu’avec les organismes de réglementation et d’accès au Royaume-Uni pour offrir l’histotripsie aux patients à travers le pays, dont beaucoup disposent de peu d’options. Cette avancée s’appuie sur notre solide bilan clinique aux États-Unis et sur notre base croissante de données cliniques sur la scène internationale. »
Depuis l’autorisation De Novo de la FDA obtenue en octobre 2023, le système Edison a été adopté dans d’importants centres universitaires et hôpitaux à travers les États-Unis, notamment dans des réseaux de santé intégrés et des hôpitaux communautaires également désireux d’offrir ce traitement novateur et non invasif à leurs patients. D’autres essais cliniques sont en cours afin d’élargir les indications de l’histotripsie, notamment pour le traitement non invasif des tumeurs rénales (essai HOPE4KIDNEY NCT05820087) et des tumeurs pancréatiques (essai GANNON NCT06282809), en vue de futures demandes d’autorisation réglementaire pour ces deux indications.
L'entreprise estime que les relations cliniques solides qu'elle a nouées au Royaume-Uni, grâce aux multiples essais cliniques pionniers menés ces dernières années sur le foie et le rein, contribueront à accélérer l'adoption de l'histotripsie dans les principaux centres de soins britanniques.
Dans le cadre de l'autorisation UCNA, HistoSonics travaillera avec la MHRA pour évaluer les résultats des patients et collecter et analyser régulièrement des données réelles sur les performances et la sécurité des dispositifs dans le cadre d'un programme de surveillance post-commercialisation. HistoSonics cherche simultanément à obtenir l'approbation réglementaire européenne par le biais du processus de conformité européenne (marquage CE), ce qui favorisera une plus forte disponibilité commerciale au Royaume-Uni et en Europe.
Déclaration d'utilisation prévue pour le Royaume-Uni :
Le système Edison est conçu pour la destruction mécanique non invasive des tumeurs hépatiques, dont la destruction partielle ou complète de tumeurs hépatiques non résécables par histotripsie. Cela inclut les cancers liés à un carcinome hépatique primitif ainsi que les cas de métastases hépatiques. L’appareil doit uniquement être utilisé par des personnes ayant suivi une formation dispensée par HistoSonics Inc., et son utilisation doit être guidée par le jugement clinique d’un médecin dûment formé. Les utilisateurs doivent lire le présent guide afin de bien comprendre les avertissements, les précautions et le résumé des essais cliniques, dont les effets indésirables signalés.
Le système Edison n'a pas été évalué pour le traitement d'une maladie spécifique, y compris, mais sans s'y limiter, le cancer, ni pour l'évaluation de résultats spécifiques liés au cancer (tels que la progression locale de la tumeur, la survie à 5 ans ou la survie globale).
Déclaration d'utilisation prévue pour les États-Unis :
Le système Edison est conçu pour la destruction mécanique non invasive des tumeurs hépatiques, dont la destruction partielle ou complète de tumeurs hépatiques non résécables par histotripsie. La FDA n’a pas évalué le système Edison pour le traitement d’une quelconque maladie, y compris – mais sans s’y limiter – le cancer, ni évalué de résultats cliniques spécifiques liés au cancer (tels que la progression locale de la tumeur, la survie à cinq ans ou la survie globale). Le système doit uniquement être utilisé par des médecins ayant suivi une formation dispensée par HistoSonics, et son utilisation doit être guidée par le jugement clinique d’un médecin dûment formé. Veuillez consulter le mode d’emploi de l’appareil pour obtenir la liste complète des avertissements, des précautions et un résumé des résultats des essais cliniques, notamment les effets indésirables signalés.
À propos de HistoSonics
HistoSonics est une société privée de dispositifs médicaux ayant mis au point une thérapie exclusive par faisceau sonique et une plateforme non invasive basées sur la science de l'histotripsie, un mécanisme d'action innovant qui a recours à des ultrasons focalisés pour liquéfier et détruire mécaniquement des tumeurs et des tissus indésirables. L'entreprise concentre actuellement ses efforts sur la commercialisation de son système de traitement hépatique Edison aux États-Unis et sur certains marchés mondiaux spécifiques tout en élargissant les applications de l'histotripsie à d'autres organes comme les reins, le pancréas, etc. HistoSonics possède des bureaux à Ann Arbor dans le Michigan et à Minneapolis dans le Minnesota. Pour plus d'informations sur le système d'histotripsie Edison, rendez-vous sur : www.histosonics.com/. Pour obtenir des informations sur les patients, veuillez consulter le site suivant : www.myhistotripsy.com/.
« L'essai pivot à bras unique #HOPE4LIVER pour l'histotripsie des tumeurs hépatiques primaires et métastatiques : 1-year update of clinical outcomes » publié dans Annals of Surgery par Ziemlewicz, et.al. est placé sous licence CC BY-NC-ND.
Le texte du communiqué issu d’une traduction ne doit d’aucune manière être considéré comme officiel. La seule version du communiqué qui fasse foi est celle du communiqué dans sa langue d’origine. La traduction devra toujours être confrontée au texte source, qui fera jurisprudence.
Contacts
Pour les demandes des médias
Personne-ressource pour les médias :
Josh King
Vice-Président du Marketing
Email : Joshua.king@histosonics.com
Téléphone : 608.332.8124
Kimberly Ha
KKH Advisors
917-291-5744
kimberly.ha@kkhadvisors.com

